Les protéines C1S, C4d et facteur H du système du complément activent la progression de certains cancers, comme le montre le groupe de Lubka Roumenina dans deux articles publiés en Mai dans Cancer Immunology Research.
L’équipe de Lubka Roumenina montre que certaines protéines du système du complément (un élément de l’immunité innée) jouent un rôle dans la progression de certains cancers du rein (carcinome rénal à cellules claires, ccRCC) et du poumon (adénocarcinome) ainsi que dans le pronostic d’évolution de ces cancers. Ces résultats suggèrent que le système du complément pourrait constituer une nouvelle cible thérapeutique pour ces cancers en particulier. Ils ont été publiés dans deux articles dans le même numéro de consécutifs dans Cancer Immunology Research.
Le système du complément est un groupe de 35 protéines qui agissent en cascade dans la réponse immunitaire pour éliminer les agents pathogènes lors d’une infection. Lorsqu’un agent pathogène est détecté par le système du complément, les protéines qui le constituent induisent une inflammation, une opsonisation (dépôts de molécules spécifiques sur la cellule en vue de sa dégradation) et une lyse (destruction) cellulaire. Ce sont les fonctions classiques ou « canoniques » du complément.
Depuis quelques années, différentes études ont montré que le complément présente des fonctions « non-canoniques » via certaines protéines qui pourraient jouer un rôle dans la progression des tumeurs.
L’équipe de Lubka Roumenina s’est intéressée à ces fonctions non-canoniques via deux protéines du complément : C1s, une protéase qui agit au début de la cascade en clivant d’autres protéines pour les rendre actives dans le processus immunitaire, et FH, un régulateur de l’activité du complément.
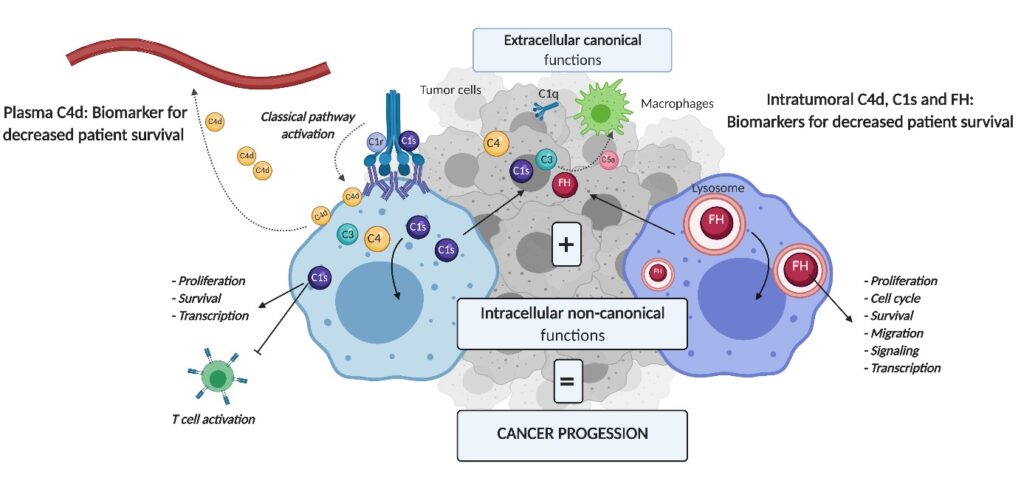
C1s agit en particulier en clivant la protéine C4 (autre protéine du complément), ce qui libère un fragment C4d de cette protéine. Daugan, Revel et leurs collègues ont découvert qu’une quantité élevée de C4d dans le plasma et sur les cellules tumorales de patients atteints de cancer du rein (carcinome rénal à cellules claires, ccRCC) est associée à un mauvais pronostic. Un niveau élevé de C4d apparait donc comme un biomarqueur de mauvais pronostic pour ces tumeurs.
Les chercheurs ont observé un effet protumoral associé à une localisation inhabituelle de FH au niveau des lysosomes et de C1s au niveau du cytoplasme chez des patients atteints de ccRCC et d’adénocarcinome pulmonaire (ADC). Ils montrent ainsi pour la première fois une fonction intracellulaire des protéines du complément, connues pour agir normalement dans l’espace extracellulaire.
Pour C1s comme pour FH, les protéines apparaissent surexprimées dans les tumeurs. La forte expression de C1s dans les tumeurs humaines a été corrélée à une augmentation de l’infiltration et de l’épuisement des cellules T, qui ne sont plus capables de détruire les cellules tumorales.
Pour mieux comprendre l’action de C1s et FH dans les cellules tumorales, les chercheurs ont créé des lignées où les gènes de ces deux protéines ont été inactivés, et où ces protéines sont par conséquent absentes.
L’inhibition de C1s et de FH dans les cellules tumorales in vitro a modifié le programme de transcription, diminué la prolifération et augmenté la mortalité des cellules. L’absence de ces protéines semble donc avoir un effet anti-tumoral.
Le mode d’action des deux protéines semble être différent. La suppression de C1s a rendu les cellules tumorales capables d’induire l’activation des cellules T dans un modèle de co-culture, ce qui restaure leur capacité à détruire les cellules tumorales. L’inhibition de la FH a entraîné une diminution de la prolifération, due à un arrêt du cycle cellulaire, et une augmentation de la mortalité. De plus, en absence de FH, la migration des cellules est réduite, probablement en raison d’une morphologie altérée, ce qui pourrait réduire la production de métastases.
Ces effets semblent spécifiques du type de tumeur considéré car aucune modification n’a été observée dans les cellules endothéliales (HUVECs) ou les cellules squameuses du cancer du poumon lors de la suppression d’expression de la FH.
Par conséquent, la surexpression de C1s et de FH par les cellules tumorales apparait comme un nouveau mécanisme d’échappement qui favorise la progression tumorale, en synergie avec le rôle de promotion des tumeurs du complément déjà connu pour le ccRCC et l’adénocarcinome du poumon. Grâce à cette connaissance des mécanismes d’action des protéines du complément et de l’impact pronostique de leur surexpression, les auteurs soulignent le fort potentiel d’une thérapie ciblant le système du complément dans des sous-groupes sélectionnés de patients cancéreux.
Article 1: Complement C1s and C4d as prognostic biomarkers in renal cancer: emergence of noncanonical functions of C1s.
Daugan et al, Cancer Immunology Research, May 2021
Article 2:
Intracellular Factor H drives tumor progression independently of the complement cascade.Daugan et al, Cancer Immunology Research, May 2021
Equipe Inflammation, Complément et Cancer
Ces résultats ont fait l’objet d’un article sur le site de l’Inserm IdF. Lire l’article

